Metoda pengambilan contoh air limbah sesuai SNI 6989.59:2008
Dalam rangka menyeragamkan teknik pengambilan contoh air limbah sebagaimana telah ditetapkan dalam Keputusan Menteri Negara Lingkungan Hidup Nomor 02 Tahun 1988 tentang Baku Mutu Air dan Keputusan Menteri Negara Lingkungan Hidup Nomor 37 Tahun 2003 tentang Metoda Analisis Kualitas Air Permukaan dan Pengambilan Contoh Air Permukaan, maka dibuatlah Standar Nasional Indonesia (SNI) tentang Air dan air limbah Bagian 59: Metode pengambilan contoh air limbah. SNI ini diterapkan untuk teknik pengambilan contoh air limbah sebagaimana yang tercantum di dalam Keputusan Menteri tersebut.
Metoda ini digunakan untuk pengambilan contoh air guna keperluan pengujian sifat fisika dan kimia air limbah.
Istilah dan definisi
air limbah, sisa dari suatu hasil usaha dan atau kegiatan yang berwujud cair
kualitas air limbah, sifat-sifat air limbah yang ditunjukkan dengan besaran, nilai atau kadar bahan pencemar atau komponen lain yang terkandung didalamnya
contoh sesaat (grab sample), air limbah yang diambil sesaat pada satu lokasi tertentu
contoh gabungan waktu, campuran contoh yang diambil dari satu titik pada waktu yang berbeda, dengan volume yang sama
contoh gabungan tempat, campuran contoh yang diambil dari titik yang berbeda pada waktu yang sama, dengan volume yang sama
contoh gabungan waktu dan tempat, campuran contoh yang diambil dari beberapa titik dalam satu lokasi pada waktu yang berbeda, dengan volume yang sama
contoh duplikat, contoh yang diambil dari titik pengambilan yang sama dengan rentang waktu antar pengambilan yang sekecil mungkin, duplikat contoh digunakan untuk menguji ketelitian tata kerja pengambilan contoh
contoh yang diperkaya (spike sample), contoh yang ditambah dengan standar yang bersertifikat dalam jumlah tertentu untuk keperluan pengendalian mutu
contoh yang terbelah (split sample), contoh dikumpulkan dalam satu wadah, dihomogenkan dan dibagi menjadi dua atau lebih sub contoh dan diperlakukan seperti contoh, selanjutnya dikirim ke beberapa laboratorium yang berbeda
blanko matrik, media bebas analit yang mempunyai matrik hampir sama dengan contoh yang akan diambil
blanko media, media yang digunakan untuk mendeteksi adanya kontaminasi pada media yang digunakan dalam pengambilan contoh
blanko perjalanan, media yang digunakan untuk mengukur kontaminasi yang mungkin terjadi selama pengambilan dan transportasi contoh
Kebutuhan Oksigen Biologi/KOB (Biologycal Oxcygen Demand, BOD), kebutuhan oksigen biokimiawi bagi proses deoksigenasi dalam suatu perairan atau air limbah
Kebutuhan Oksigen Kimiawi/KOK (Chemical Oxcygen Demand COD), kebutuhan oksigen kimiawi bagi proses deoksigenasi dalam suatu perairan atau air limbah
n utrien, senyawa yang dibutuhkan oleh organisme yang meliputi fosfat, nitrogen, nitrit, nitrat dan amonia
titik pengambilan contoh air limbah, tempat pengambilan contoh yang mewakili kualitas air limbah
bak equalisasi, bak penampungan air limbah yang bertujuan untuk menghomogenkan beban dan pengaturan aliran air limbah
Peralatan
Persyaratan alat pengambil contoh
Alat pengambil contoh harus memenuhi persyaratan sebagai berikut:
a) terbuat dari bahan yang tidak mempengaruhi sifat contoh;
b) mudah dicuci dari bekas contoh sebelumnya;
c) contoh mudah dipindahkan ke dalam botol penampung tanpa ada sisa bahan tersuspensi di dalamnya;
d) mudah dan aman di bawa;
e) kapasitas alat tergantung dari tujuan pengujian.
Jenis alat pengambil contoh
a) Alat pengambil contoh sederhana
Alat pengambil contoh sederhana dapat berupa ember plastik yang dilengkapi dengan tali atau gayung plastik yang bertangkai panjang.
CATATAN Dalam praktiknya, alat sederhana ini paling sering digunakan dan dipakai untuk mengambil air permukaan atau air sungai kecil yang relatif dangkal.
Keterangan gambar:
A adalah pengambil contoh terbuat dari polietilen
B adalah handle (tipe teleskopi yang terbuat dari aluminium atau stanlestil
Gambar 1 Contoh alat pengambil contoh gayung bertangkai panjang
Gambar 2 Contoh botol biasa secara langsung
b) botol biasa yang diberi pemberat yang digunakan pada kedalaman tertentu.
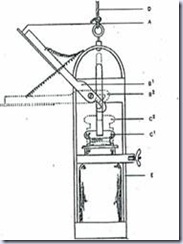 | Keterangan gambar:
A adalah pengait
B1 adalah tuas posisi tertutup
B2 adalah tuas posisi terbuka
C1 adalah tutup gelas botol contoh posisi tertutup
C2 adalah tutup gelas botol contoh posisi terbuka
D adalah tali penggantung
E adalah rangka metal botol contoh |
Gambar 3 Contoh alat pengambil air Bbotol biasa dengan pemberat
Alat pengambil contoh air otomatis
Alat ini dilengkapi alat pengatur waktu dan volume yang diambil, digunakan untuk contoh gabungan waktu dan air limbah, agar diperoleh kualitas air rata-rata selama periode tertentu
Gam bar 4 Alat pengambil contoh air otomatis
Alat pengukur parameter lapangan
Peralatan yang perlu dibawa antara lain:
a) DO meter atau peralatan untuk metode Winkler;
b) pH meter;
c) turbidimeter;
d) konduktimeter;
e) termometer; dan
f) 1 set alat pengukur debit.
CATATAN Alat lapangan sebelum digunakan perlu dilakukan kalibrasi.
Alat pendingin, Alat ini dapat menyimpan contoh pada 4C 2C, digunakan untuk menyimpan contoh untuk pengujian sifat fisika dan kimia.
Alat ekstraksi (corong pemisah), Corong pemisah terbuat dari bahan gelas atau teflon yang tembus pandang dan mudah memisahkan fase pelarut dari contoh.
Alat penyaring, Alat ini dilengkapi dengan pompa isap atau pompa tekan serta dapat menahan saringan yang mempunyai ukuran pori 0,45 m.
Bahan
Bahan kimia untuk pengawet. Bahan kimia yang digunakan untuk pengawet harus memenuhi persyaratan bahan kimia untuk analisis dan tidak mengganggu atau mengubah kadar zat yang akan di uji (lihat Lampiran B).
Wadah contoh
Persyaratan wadah contoh, Wadah yang digunakan untuk menyimpan contoh harus memenuhi persyaratan sebagai berikut:
a) terbuat dari bahan gelas atau plastik poli etilen (PE) atau poli propilen (PP) atau teflon (Poli Tetra Fluoro Etilen, PTFE);
b) dapat ditutup dengan kuat dan rapat;
c) bersih dan bebas kontaminan;
d) tidak mudah pecah;
e) tidak berinteraksi dengan contoh.
Persiapan wadah contoh
Lakukan langkah-langkah persiapan wadah contoh, sebagai berikut:
a) Untuk menghindari kontaminasi contoh di lapangan, seluruh wadah contoh harus benarbenar dibersihkan di laboratorium sebelum dilakukan pengambilan contoh.
b) Wadah yang disiapkan jumlahnya harus selalu dilebihkan dari yang dibutuhkan, untuk jaminan mutu, pengendalian mutu dan cadangan.
c) Jenis wadah contoh dan tingkat pembersihan yang diperlukan tergantung dari jenis contoh yang akan diambil, sebagai berikut:
Wadah contoh untuk pengujian senyawa organik yang mudah menguap (Volatile Organic Compound, VOC)
Siapkan wadah contoh untuk senyawa organik yang mudah menguap, dengan langkah kerja sebagai berikut:
a) cuci gelas vial, tutup dan septum dengan deterjen. Bilas dengan air biasa dan kemudian bilas dengan air bebas analit;
b) bilas dengan metanol berkualitas analisis dan dikeringkan selama 1 jam;
c) keluarkan vial dan biarkan mendingin dalam posisi terbalik di atas lembaran aluminium foil;
d) setelah vial dingin, putar tutup dan septum untuk menutup vial tersebut.
CATATAN Untuk mencegah kontaminasi saat pencucian wadah contoh yang akan digunakan untuk analisa organik, harus dihindari penggunaan sarung tangan plastik atau karet dan sikat.
Wadah contoh untuk pengujian senyawa organik yang dapat diekstraksi
Siapkan wadah contoh untuk senyawa organik yang dapat diekstraksi, dengan langkah kerja sebagai berikut:
-
cuci botol gelas dan tutup dengan deterjen. Bilas dengan air kemudian dengan air bebas analit;
-
masukkan 10 mL aseton berkualitas analisis ke dalam botol dan rapatkan tutupnya, kemudian kocok botol dengan baik agar aseton tersebar merata dipermukaan dalam botol serta mengenai lining teflon dalam tutup.
-
buka tutup botol dan buang aseton dan biarkan botol mengering dan kemudian kencangkan tutup botol agar tidak terjadi kontaminasi baru.
Wadah contoh untuk pengujian logam total dan terlarut
Siapkan wadah contoh untuk pengujian logam total dan terlarut, dengan langkah kerja sebagai berikut:
a) cuci botol gelas atau plastik dan tutupnya dengan deterjen kemudian bilas dengan air bersi h.
b) bilas dengan asam nitrat (HNO3) 1:1, kemudian bilas lagi dengan air bebas analit sebanyak 3 kali dan biarkan mengering, setelah kering tutup botol dengan rapat.
Wadah contoh untuk pengujian KOB, KOK dan nutrien
Siapkan wadah contoh untuk pengujian KOB, KOK dan nutrien, dengan langkah kerja sebagai berikut:
a) cuci botol dan tutup dengan deterjen bebas fosfat kemudian bilas dengan air bersih;
b) cuci botol dengan asam klorida (HCl) 1:1 dan bilas lagi dengan air bebas analit sebanyak 3 kali dan biarkan mengering, setelah kering tutup botol dengan rapat.
Wadah contoh untuk anorganik non-logam
Siapkan wadah contoh untuk pengujian anorganik non-logam, dengan langkah kerja sebagai berikut:
a) cuci botol dan tutup dengan deterjen, bilas dengan air bersih kemudian bilas dengan air bebas analit sebanyak 3 kali dan biarkan hingga mengering;
b) setelah kering tutup botol dengan rapat.
Pencucian wadah contoh
Lakukan pencucian wadah contoh sebagai berikut:
a) Peralatan harus dicuci dengan deterjen dan disikat untuk menghilangkan partikel yang menempel di permukaan;
b) Bilas peralatan dengan air bersih hingga seluruh deterjen hilang;
c) Bila peralatannya terbuat dari bahan non logam, maka cuci dengan asam HNO3 1:1, kemudian dibilas dengan air bebas anal it;
d) Biarkan peralatan mengering di udara terbuka;
e) Peralatan yang telah dibersihkan diberi label bersih-siap untuk pengambilan contoh.
Volume contoh
Volume contoh yang diambil untuk keperluan pengujian di lapangan dan laboratorium bergantung dari jenis pengujian yang diperlukan (lihat Lampiran B).
7 Tipe contoh
Beberapa tipe contoh air limbah:
a) contoh sesaat (grab sample);
b) contoh gabungan waktu (composite samples);
c) contoh gabungan tempat (integrated samples);
d) contoh gabungan waktu dan tempat.
Lokasi dan titik pengambilan contoh
Pemilihan lokasi pengambilan contoh
a) Lokasi pengambilan contoh air limbah industri harus mempertimbangkan ada atau tidak adanya Instalasi Pengolahan Air Limbah (IPAL).
b) Contoh harus diambil pada lokasi yang telah mengalami pencampuran secara sempurna.
Penentuan lokasi pengambilan contoh
Lokasi pengambilan contoh dilakukan berdasarkan pada tujuan pengujian, sebagai berikut:
Untuk keperluan evaluasi efisiensi Instalasi Pengolahan Air Limbah (IPAL)
a) Contoh diambil pada lokasi sebelum dan setelah IPAL dengan memperhatikan waktu tinggal (waktu retensi).

 Gambar 5 Contoh lokasi pengambilan contoh sebelum dan setelah IPAL
Gambar 5 Contoh lokasi pengambilan contoh sebelum dan setelah IPAL
b) Titik lokasi pengambilan contoh pada inlet (titik 2, Gambar 5)
1) Dilakukan pada titik pada aliran bertubulensi tinggi agar terjadi pencampuran dengan baik, yaitu pada titik dimana limbah mengalir pada akhir proses produksi menuju ke IPAL.
2) Apabila tempat tidak memungkinkan untuk pengambilan contoh maka dapat ditentukan lokasi lain yang dapat mewakili karakteristik air limbah.
c) Titik lokasi pengambilan contoh pada outlet (titik 3, Gambar 5)
Pengambilan contoh pada outlet dilakukan pada lokasi setelah IPAL atau titik dimana air limbah yang mengalir sebelum memasuki badan air penerima (sungai).
Untuk keperluan pengendalian pencemaran air
Untuk keperluan pengendalian pencemaran air, contoh diambil pada 3 (tiga) lokasi:
a) Pada perairan penerima sebelum tercampur limbah (upstream) (titik 4, Gambar 5).
b) Pada saluran pembuangan air limbah sebelum ke perairan penerima (titik 3, Gambar 5).
c) Pada perairan penerima setelah bercampur dengan air limbah (downsream), namun belum tercampur atau menerima limbah cair lainnya (titik 5, Gambar 5).
Untuk industri yang belum memiliki IPAL
Air limbah industri dengan proses kontinyu berasal dari satu saluran pembuangan
Jika tidak terdapat bak ekualisasi
a) Kualitas air limbah tidak berfluktuasi, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara sesaat (grab sampling).
b) Kualitas air limbah berfluktuasi akibat proses produksi, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara komposit waktu.
Jika terdapat bak ekualisasi
Pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara sesaat (grab sampling).
Air limbah industri dengan proses batch berasal dari satu saluran pembuangan
Jika tidak terdapat bak equalisasi
Kualitas air limbah berfluktuasi akibat proses produksi, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara komposit waktu dan proporsional pada saat pembuangan dilakukan.
Jika terdapat bak equalisasi
Pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara sesaat (grab sampling).
Air limbah industri dengan proses kontinyu berasal dari beberapa saluran pembuangan
Jika tidak terdapat bak equalisasi
a) Kualitas air limbah tidak berfluktuasi dan semua saluran pembuangan limbah dari beberapa sumber sebelum masuk perairan penerima limbah disatukan, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara sesaat.
b) Kualitas air limbah tidak berfluktuasi dan semua saluran pembuangan limbah dari beberapa sumber sebelum masuk perairan penerima limbah tidak disatukan, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara komposit tempat dengan mempertimbangkan debit.
c) Kualitas air limbah berfluktuasi akibat proses produksi dan semua saluran pembuangan limbah dari beberapa sumber sebelum masuk perairan penerima limbah disatukan, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara komposit waktu.
d) Kualitas air limbah berfluktuasi akibat proses produksi dan semua saluran pembuangan limbah dari beberapa sumber sebelum masuk perairan penerima limbah tidak disatukan, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara komposit waktu dan tempat.
Jika terdapat bak equalisasi
Kualitas air limbah berfluktuasi atau tidak berfluktuasi akibat proses produksi, semua air limbah dari masing-masing proses disatukan dan dibuang melalui bak equalisasi, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara sesaat (grab sampling).
Air limbah industri dengan proses batch berasal dari beberapa saluran pembuangan
Jika tidak terdapat bak equalisasi
a) Kualitas air limbah berfluktuasi akibat proses produksi dan semua saluran pembuangan limbah dari beberapa sumber sebelum masuk perairan penerima limbah disatukan, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara komposit waktu.
b) Kualitas air limbah berfluktuasi akibat proses produksi dan semua saluran pembuangan limbah dari beberapa sumber sebelum masuk perairan penerima limbah tidak disatukan, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara komposit waktu dan tempat dengan mempertimbangkan debit.
Jika terdapat bak equalisasi
Kualitas air limbah berfluktuasi atau sangat berfluktuasi akibat proses produksi, semua air limbah dari masing-masing proses disatukan dan dibuang melalui bak equalisasi, maka pengambilan contoh dilakukan pada saluran sebelum masuk ke perairan penerima air limbah, dengan cara sesaat (grab sampling).
Untuk industri yang memiliki IPAL
Lakukan pengambilan contoh pada saluran pembuangan air limbah sebelum ke perairan penerima (titik 3, Gambar 1).
CARA PENGAMBILAN CONTOH
Pengambilan contoh untuk pengujian kualitas air
a) siapkan alat pengambil contoh sesuai dengan saluran pembuangan;
b) bilas alat dengan contoh yang akan diambil, sebanyak 3 (tiga) kali;
c) ambil contoh sesuai dengan peruntukan analisis dan campurkan dalam penampung sementara, kemudian homogenkan;
d) masukkan ke dalam wadah yang sesuai peruntukan analisis;
e) lakukan segera pengujian untuk parameter suhu, kekeruhan dan daya hantar listrik, pH dan oksigen terlarut yang dapat berubah dengan cepat dan tidak dapat diawetkan;
f) hasil pengujian parameter lapangan dicatat dalam buku catatan khusus;
g) pengambilan contoh untuk parameter pengujian di laboratorium dilakukan pengawetan seperti pada Lampiran B.
CATATAN Untuk contoh yang akan di uji kandungan senyawa organiknya dan logam, hendaknya tidak membilas alat 3 kali dengan contoh air, tetapi digunakan wadah yang bersih dan siap pakai.
Pengambilan contoh untuk pengujian oksigen terlarut Pengambilan contoh dapat dilakukan dengan dua cara, yaitu: Cara langsung
a) Gunakan alat DO meter.
b) Cara pengoperasian alat, lihat petunjuk kerja alat.
c) Nilai oksigen terlarut dapat langsung terbaca.
Cara tidak langsung
Cara umum
Pengukuran oksigen terlarut dilakukan dengan cara titrasi, sebagai berikut:
a) siapkan botol KOB yang bersih dengan volume yang diketahui serta dilengkapi dengan tutup asah;
b) celupkan botol dengan hati-hati ke dalam air dengan posisi mulut botol searah dengan aliran air, sehingga air masuk ke dalam botol dengan tenang, atau dapat pula dengan menggunakan sifon;
c) isi botol sampai penuh dan hindarkan terjadinya turbulensi dan gelembung udara selama pengisian, kemudian botol ditutup;
d) contoh siap untuk dianalisa.
Cara khusus
Tahapan pengambilan contoh dengan cara alat khusus, dilakukan sebagai berikut:
a) siapkan botol KOB yang bersih dengan volume yang diketahui serta dilengkapi dengan tutup asah;
b) masukkan botol ke dalam alat khusus (lihat Gambar 3);
c) ikuti prosedur pemakaian alat tersebut;
d) Alat pengambil contoh untuk pengujian oksigen terlarut ini dapat ditutup segera setelah terisi penuh.
Pengambilan contoh untuk pengujian senyawa organik mudah menguap (Volatile Organic Compound, VOC)
Tahapan pengambilan contoh untuk pengujian senyawa VOC, dilakukan sebagai berikut:
a) selama melakukan pengambilan contoh untuk pengujian senyawa VOC, sarung tangan lateks harus terus dipakai, sarung tangan plastik atau sintetis tidak boleh digunakan;
b) saat mengambil contoh untuk analisa VOC, contoh tidak boleh terkocok untuk menghindari aerasi, aerasi contoh akan menyebabkan hilangnya senyawa volatil dari dalam contoh;
c) bila menggunakan alat bailer (Gambar 5)
1) jangan menyentuh bagian dalam septa, buka vial VOC 40 mL dan masukkan contoh secara perlahan ke dalam vial hingga terbentuk convex meniscus di puncak vial;
2) tutup vial secara hati-hati dan tidak boleh ada udara dalam vial;
3) balikkan vial dan tahan;
4) bila terlihat gelembung dalam vial, contoh harus diganti dan ambil contoh yang baru.
CATATAN Contoh VOC biasanya dibuat dalam dua atau tiga buah contoh, tergantung kebutuhan laboratorium; ulangi pengambilan contoh bila diperlukan.
 | Line for lowering and lifting
Rigid teflon tubing
Glass marble-ball and seat valv Teflon extruded rod |
Gambar 5 Alat pengambil contoh untuk parameter VOC tipe Bailer
d) seluruh vial diberi label yang jelas, bila menggunakan vial bening bungkus dengan aluminium foil dan simpan dalam tempat pendingin;
e) bila air limbah mengandung residual klorin tambahkan 80 mg Na2SO3 ke dalam 1 L contoh;
f) contoh VOC karena sifatnya yang volatil, maka pengambila contoh dilakukan secara sesaat (grab contoh), bukan komposit.
Pengambilan contoh untuk pengujian senyawa aromatik dan akrolein dan akrilonitril
Tahapan pengambilan contoh untuk pengujian senyawa aromatik dan akrolein dan akrilonitril, dilakukan sebagai berikut:
a) lakukan pengambilan contoh seperti pada butir 8.3 untuk pengujian senyawa aromatik, tetapi vialnya hanya diisi setengah dan sisanya ditambahkan dengan asam dalam jumlah yang diperlukan;
b) untuk pengujian senyawa akrolein dan akrilonitril contoh diatur hingga pH 4 - 5.
c) contoh akrolein dan akrilonitril harus dianalisa dalam waktu 3 hari setelah pengambilan contoh.
Pengambilan contoh untuk pengujian senyawa organik yang dapat diekstraksi
Tahapan pengambilan contoh untuk pengujian senyawa organik yang dapat diekstraksi, dilakukan sebagai berikut:
a) ambil contoh dengan menggunakan bailer;
d) buka tutup botol gelas 1000 mL secara hati-hati agar tidak menyentuh bagian dalam dari tutup;
e) isi botol hingga 1 cm dari puncak botol;
f) bila satu bailer tidak cukup untuk mengisi botol, tutup botol untuk menghindari kontaminasi contoh dan ambil lagi contoh, dan lanjutkan pengisian botol;
g) bila contoh memerlukan analisa pestisida, pH contoh harus diatur antara pH 5 - 9 dengan menggunakan H2SO4 atau NaOH.
Pengambilan contoh untuk pengujian total logam dan terlarut
Tahapan pengambilan contoh untuk pengujian total logam dan terlarut, dilakukan sebagai berikut:
a) bilas botol contoh dan tutupnya dengan contoh yang akan dianalisa;
b) buang air pembilas dan isi botol dengan sampel hingga beberapa cm di bawah puncak botol agar masih tersedia ruang untuk menambahkan pengawet dan melakukan pengocokan.
CATATAN Pengambilan contoh untuk pengujian logam terlarut, lakukan penyaringan contoh.
PENGUJIAN PARAMETER LAPANGAN
Pengujian parameter lapangan yang dapat berubah dengan cepat, dilakukan langsung setelah pengambilan contoh. Parameter tersebut antara lain; pH (SNI 06-6989.11-2004), suhu (SNI 06-6989.23-2005), daya hantar listrik (SNI 06-6989.1-2004), alkalinitas (SNI 06- 2420-1991), asiditas (SNI 06-2422-1991) dan oksigen terlarut (SNI 06-6989.14-2004).
Penyaringan contoh
Bila analisis tidak dapat segera dilakukan, maka perlu dilakukan penyaringan di lapangan untuk pemeriksaan parameter yang terlarut. Cara penyaringan dapat dilakukan sebagai berikut:
a) contoh yang akan disaring diambil sesuai keperluannya;
b) masukkan contoh tersebut ke dalam alat penyaring yang telah dilengkapi saringan yang mempunyai ukuran pori 0,45 m dan saring sampai selesai;
c) air saringan ditampung dalam wadah yang telah disiapkan sesuai keperluannya.
Pengawetan contoh
Pengawetan contoh dilakukan apabila pemeriksaan tidak dapat langsung dilakukan setelah pengambilan contoh (lihat Lampiran B).
Jaminan mutu dan pengendalian mutu
Jaminan mutu
a) Gunakan alat gelas bebas kontaminasi.
b) Gunakan alat ukur yang terkalibrasi.
c) Dikerjakan oleh petugas pengambil contoh yang kompeten.
Pengendalian mutu
Untuk menjamin kelayakan pengambilan contoh maka kemampuan melacak seluruh kejadian selama pelaksanaan pengambilan contoh harus dijamin.
Kontrol akurasi dapat dilakukan dengan beberapa cara berikut ini: Contoh split
a) Contoh terbelah diambil dari satu titik dan dimasukkan ke dalam wadah yang sesuai.
b) Contoh dicampur sehomogen mungkin serta dipisahkan ke dalam dua wadah yang telah disiapkan.
c) Kedua contoh tersebut diawetkan dan mendapatkan perlakuan yang sama selama perjalanan dan preparasi serta analisa laboratorium.
Contoh duplikat
a) Contoh diambil dari titik yang sama pada waktu yang hampir bersamaan.
b) Bila contoh kurang dari lima, contoh duplikat tidak diperlukan.
c) Bila contoh diambil 5 contoh sampai dengan 10 contoh, satu contoh duplikat harus diambil.
d) Bila contoh diambil lebih dari 10 contoh, contoh duplikat adalah 10% per kelompok parameter matrik yang diambil.
Contoh blanko
a) Blanko media
1) Digunakan untuk medeteksi kontaminasi pada media yang digunakan dalam pengambilan contoh (peralatan pengambilan atau wadah).
2) Peralatan pengambilan, sedikitnya satu blanko peralatan harus tersedia untuk setiap dua puluh) contoh per kelompok parameter untuk matrik yang sama.
3) Wadah, salah satu wadah yang akan digunakan diambil secara acak kemudian diisi dengan media bebas analit dan dibawa ke lokasi pengambilan contoh. Blanko tersebut kemudian dibawa ke laboratorium untuk dianalisis.
b) Blanko perjalanan
1) Blanko digunakan apabila contoh yang diambil bersifat mudah menguap.
2) Sekurang-kurangnya satu blanko perjalanan disiapkan untuk setiap jenis contoh yang mudah menguap.
3) Berupa media bebas analit yang disiapkan di laboratorium.
4) Blanko dibawa ke lokasi pengambilan, ditutup selama pengambilan contoh dan dibawa kembali ke laboratorium.
Pelaporan
Catat pada lembar data jaminan mutu untuk setiap parameter yang diukur dan contoh yang diambil, lembar data parameter yang diukur di lapangan harus memiliki informasi sekurangkurangnya sebagai berikut:
a) Identifikasi contoh.
b) Tanggal.
c) Waktu.
d) Nama Petugas Pengambil Contoh (PPC).
e) Nilai parameter yang diukur di lapangan.
f) Analisa yang diperlukan.
g) Jenis contoh (misalnya contoh, contoh split, duplikat atau blanko).
h) Komentar dan pengamatan.